L'équipe CSS étudie les processus développementaux et métaboliques qui ont conduit à l’évolution des graines.
L’évolution de la formation de la graine a profondément contribué à la diversification et au succès écologique des plantes à graines, façonnant en fin de compte les écosystèmes terrestres modernes et, indirectement, la société humaine. Nous réexaminons l’évolution de la graine sous un angle largement négligé ces dernières années, bien qu’il ait été fo
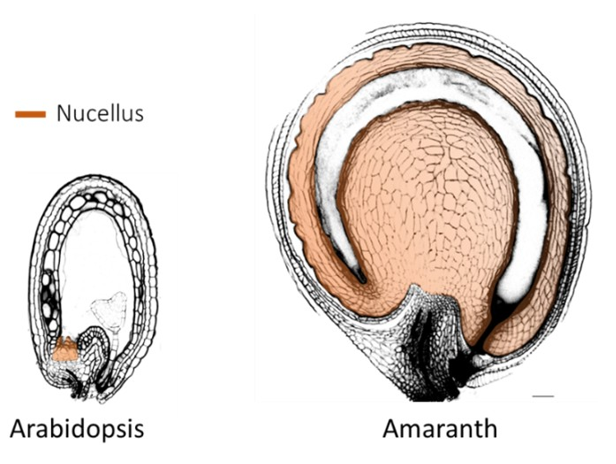 rmulé dès 1851 par Wilhelm Hofmeister, l’un des pères fondateurs de la biologie végétale. Le tissu nucellaire, responsable de la sporogenèse femelle, est passé d’un état déhiscent, comme chez les plantes sans graines où les spores sont libérées, à un état indéhiscent chez les plantes à graines, où les spores sont retenues. Ce changement du destin cellulaire du nucelle a marqué de manière décisive l’évolution des plantes à graines. La rétention des spores a nécessité l’accueil du gamétophyte femelle en développement au sein des tissus maternels. Pour faciliter ce processus, le nucelle a acquis la capacité de créer de l’espace par un processus d’élimination cellulaire, conduisant à la disparition complète de la cellule, y compris de sa paroi. Après la fécondation du gamétophyte, le nucelle organise l’organisation spatiale de la graine, donnant naissance à des architectures spécifiques à chaque espèce. Chez les gymnospermes, qui subissent un seul événement de fécondation pour produire un embryon zygotique, le nucelle est ensuite éliminé par le gamétophyte femelle, principal tissu de réserve. Chez les angiospermes, qui produisent deux produits de fécondation, l’embryon et l’endosperme, le nucelle est soit consommé par l’endosperme (graines endospermiques, comme les céréales et Arabidopsis), soit conservé (graines périspermiques, comme l’amarante) pour stocker des nutriments aux dépens de l’endosperme.
rmulé dès 1851 par Wilhelm Hofmeister, l’un des pères fondateurs de la biologie végétale. Le tissu nucellaire, responsable de la sporogenèse femelle, est passé d’un état déhiscent, comme chez les plantes sans graines où les spores sont libérées, à un état indéhiscent chez les plantes à graines, où les spores sont retenues. Ce changement du destin cellulaire du nucelle a marqué de manière décisive l’évolution des plantes à graines. La rétention des spores a nécessité l’accueil du gamétophyte femelle en développement au sein des tissus maternels. Pour faciliter ce processus, le nucelle a acquis la capacité de créer de l’espace par un processus d’élimination cellulaire, conduisant à la disparition complète de la cellule, y compris de sa paroi. Après la fécondation du gamétophyte, le nucelle organise l’organisation spatiale de la graine, donnant naissance à des architectures spécifiques à chaque espèce. Chez les gymnospermes, qui subissent un seul événement de fécondation pour produire un embryon zygotique, le nucelle est ensuite éliminé par le gamétophyte femelle, principal tissu de réserve. Chez les angiospermes, qui produisent deux produits de fécondation, l’embryon et l’endosperme, le nucelle est soit consommé par l’endosperme (graines endospermiques, comme les céréales et Arabidopsis), soit conservé (graines périspermiques, comme l’amarante) pour stocker des nutriments aux dépens de l’endosperme.L’évolution de la cohabitation entre zygote et tissus maternels dans la graine nécessite un réseau de signalisation complexe pour transmettre les signaux de fécondation, favoriser le développement d’un environnement maternel propice à l’embryogenèse et assurer une coordination spatio-temporelle précise de la croissance entre les compartiments maternels et zygotiques. Les tissus maternels de la graine ne participent pas directement à la fécondation, mais y répondent via une voie de signalisation dédiée qui transmet l’information de la fécondation. La communication zygote-maternelle doit également garantir une allocation équilibrée des ressources à la descendance, ce qui est fondamental pour le succès de la reproduction. Les tissus maternels doivent percevoir correctement la fécondation afin de fournir à la descendance suffisamment de nutriments pour assurer sa vigueur, sans pour autant épuiser excessivement la plante mère et compromettre sa survie. Ainsi, un point de contrôle maternel intègre l’état énergétique de la plante dans la voie de reconnaissance maternelle de la fécondation.
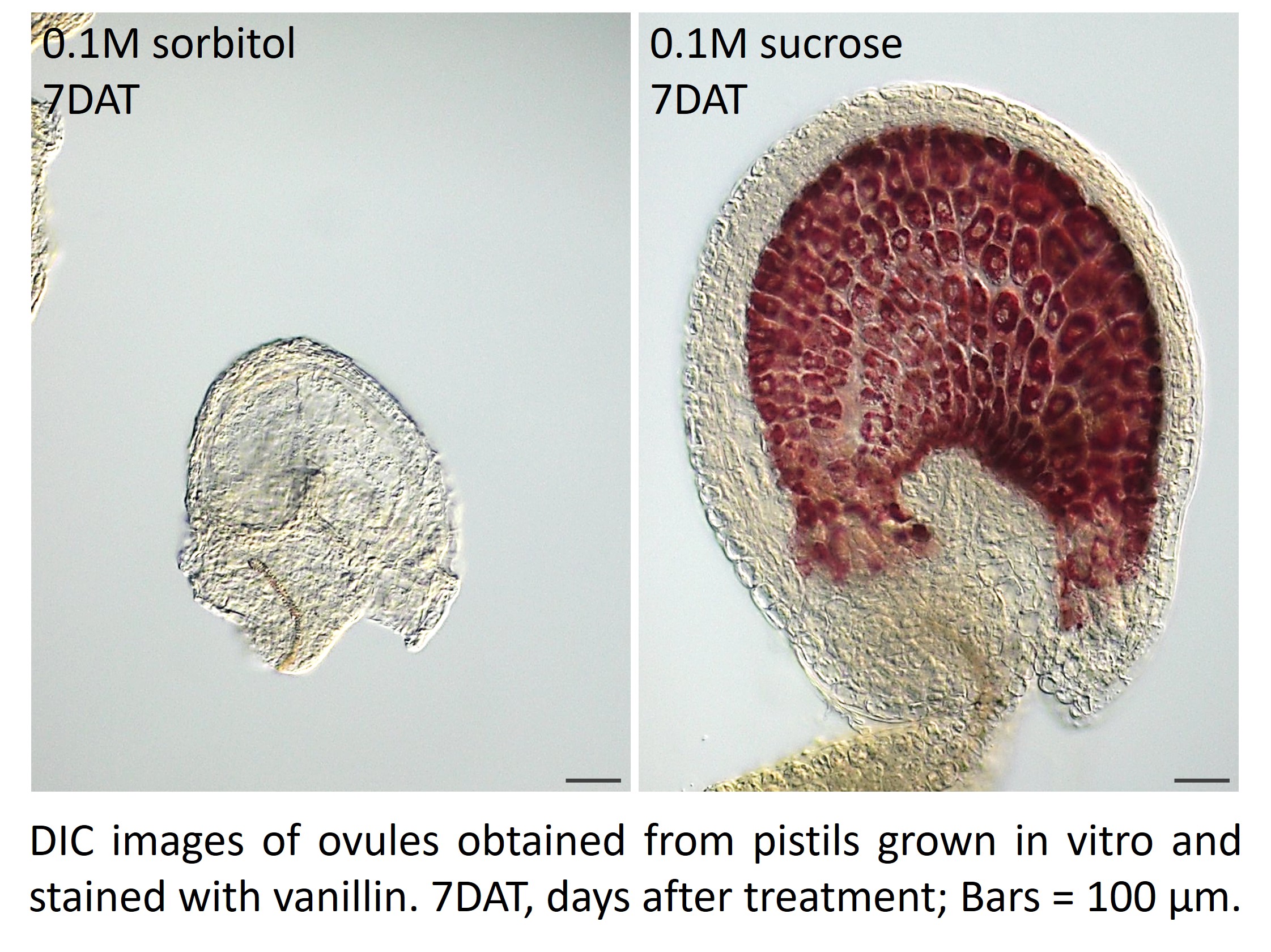
Nos travaux se concentrent sur le développement du nucelle afin d’aborder des questions fondamentales de l’évolution des graines. Nous nous intéressons particulièrement au processus d’élimination cellulaire, en mettant l’accent sur le démantèlement de la paroi cellulaire et son rôle dans la formation de différentes architectures de graines. Un second axe majeur de recherche concerne la communication entre les compartiments maternels et zygotiques, et la manière dont ces interactions influencent la structure des graines et le succès reproductif à travers les lignées végétales. Nous accordons une attention particulière à l’intégration du développement et du métabolisme au sein de voies de signalisation communes, qui coordonnent l’état énergétique avec les signaux développementaux. Nous abordons ces questions à l’aide de modèles expérimentaux complémentaires et d’outils issus de la génétique moléculaire, de la biochimie, de la biologie cellulaire et structurale, de la microscopie et de la modélisation, permettant une compréhension intégrée de ces processus à différentes échelles, moléculaire, cellulaire et évolutive.
Sélection de publications
1. Xu W., Iannaccone M., Gomez-Paez D.M., Choinard S., Lu J., Le Hir R., Dinant S., Kalmbach L., Feil R., Lunn J.E., Meyer C., Magnani E. (2025) Too much sugar makes plants ‘pregnant’: maternal sucrose signals fertilization in Arabidopsis seeds. bioRxiv 2025.05.16.654273.
2. Iannaccone M.*, Xu W.*, Gomez-Paez D.M., Choinard S., Maricchiolo E., Peaucelle A., Voxeur A., Haas K.T., Pompa A., Magnani E. (2026) A change in the cell wall status initiates the elimination of the nucellus in Arabidopsis. PNAS In press
3. Xu W., and Magnani E. (2023) An actin starry night regulates seed size. Nat Plants 9, 201-202.
4. Gómez-Páez D.M. and Magnani E. (2024) Confocal Imaging of Seeds. Methods in Molecular Biology. SpringerNature, 2830:93-104
5. Butel N., Qiu Y., Xu W., Santos-González J., Köhler C. (2024) Parental conflict driven regulation of endosperm cellularization by a family of Auxin Response Factors. Nature Plants, 10(6):1018-1026.
6. Xu W*., Sato H*., Bente H., Santos-González J., Köhler C. (2023) Endosperm cellularization failure induces a dehydration-stress response leading to embryo arrest. Plant Cell, 35(2): 874-888.
7. Lu J., Le Hir R., Gómez-Páez D.M., Coen O., Péchoux C., Jasinski S., Magnani E. (2021) The nucellus: between cell elimination and sugar transport. Plant Physiol, 185(2):478-490.
8. Magnani E. (2018) Seed evolution, a “simpler” story. Trends in Plant Science, 23(8):654-656.
9. Lu J., and Magnani E. (2018) Seed tissue and nutrient partitioning, a case for the nucellus. Plant Reprod, 31(3):309-317.
10. Xu W., Fiume E., Coen O., Longin C., Lepiniec L., Magnani E. (2016) Endosperm and Nucellus Develop Antagonistically in Arabidopsis Seeds. Plant Cell, 28(6):1343-60.

Responsable :
Enrico Magnani